金属活动性顺序表是化学学习中的重要工具,而氢在其中具有关键作用,氢的位置处于金属与非金属的交界处,其活动性适中,它能将排在它后面的金属从它们的化合物溶液中置换出来,这体现了氢的一定金属性,锌能与稀硫酸反应生成氢气,而铜不能,说明锌的活动性比铜强,氢也具有一定的非金属性,能与一些非金属元素形成化合物,金属活动性顺序表中氢的这种特殊位置和性质,使其在众多化学反应中都扮演着重要角色,对于理解化学反应的本质和规律有着重要意义。
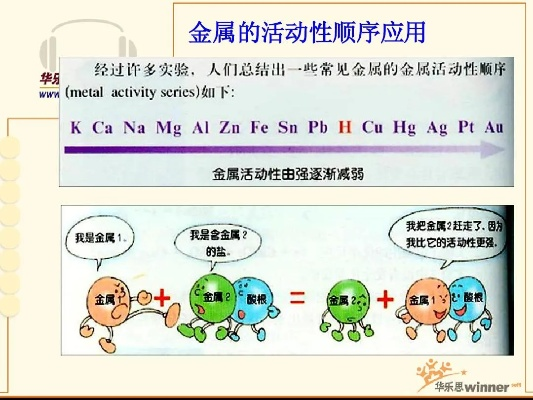
在化学的世界里,金属活动性顺序表是一个非常重要的工具,它清晰地展示了各种金属在化学反应中的活泼程度,而在这个顺序表中,氢元素虽然并非金属,却有着独特且关键的作用。
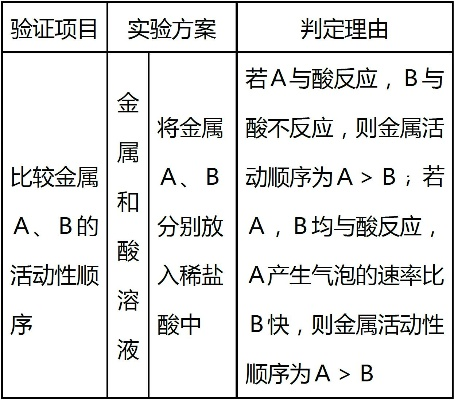
金属活动性顺序表通常按照金属元素的活动性由强到弱进行排列,排在氢前面的金属能够从酸中置换出氢气,而氢后面的金属则不能,这一特性使得氢成为了区分不同金属活泼性的重要参照点。
从置换反应的角度来看,氢的作用显而易见,当金属与酸发生反应时,氢的存在决定了反应能否进行以及反应的剧烈程度,镁、锌等活泼金属能够迅速与盐酸或稀硫酸反应,产生大量气泡(氢气),反应十分剧烈,而铜等不活泼金属则不能与酸发生这样的置换反应,通过观察金属与酸的反应现象,我们可以直观地了解到金属的活动性差异,而氢在其中起到了“标尺”的作用。
氢在金属活动性顺序表中的位置还与氧化还原反应密切相关,在氧化还原反应中,金属原子失去电子被氧化,而氢原子则有可能得到电子被还原,在铁与硫酸铜溶液的反应中,铁原子失去电子变成亚铁离子,而硫酸铜中的铜离子则得到电子被还原成铜单质,这个过程中,氢元素并没有直接参与反应,但它的存在影响了反应的方向和程度,如果反应体系中存在比氢更活泼的金属,那么氢就会以氢气的形式逸出体系,从而推动反应向生成更稳定化合物的方向进行。
金属活动性顺序表在电化学领域也有着广泛的应用,在原电池中,金属的活动性决定了电极的正负极,活动性较强的金属作为负极,发生氧化反应,而活动性较弱的金属或非金属作为正极,发生还原反应,氢在一些特殊的原电池中也可能扮演重要角色,在氢氧燃料电池中,氢气在负极被氧化,氧气在正极被还原,从而产生电能,氢的氧化反应是整个电池反应的关键步骤之一。
金属活动性顺序表中氢的作用还体现在它对金属腐蚀的影响上,金属的活动性越强,越容易与周围环境中的物质发生反应,从而导致腐蚀,而氢的存在可能会促进或抑制金属的腐蚀过程,在某些情况下,氢气的存在可能会在金属表面形成一层保护膜,从而减缓金属的腐蚀速度。
金属活动性顺序表中氢的作用不可忽视,它不仅是区分金属活泼性的重要依据,还与氧化还原反应、电化学以及金属腐蚀等诸多方面密切相关,通过对金属活动性顺序表中氢的深入理解,我们可以更好地认识金属的化学性质和化学反应规律,为化学研究和实际应用提供有力的支持,氢在其他领域如能源、材料等方面也有着重要的应用前景,值得我们进一步探索和研究。
金属活动性顺序表中的氢虽然看似普通,却蕴含着丰富的化学信息和重要的作用,它是化学领域中一个不可或缺的元素。





 京公网安备11000000000001号
京公网安备11000000000001号 沪ICP备19017178号-1
沪ICP备19017178号-1
还没有评论,来说两句吧...