《探索金属活动性顺序表完整版的奥秘》,金属活动性顺序表完整版蕴含着丰富的化学知识奥秘,它按照金属在水溶液中失去电子的能力强弱进行排列,通过对其深入探究,我们能了解不同金属与酸、盐等物质反应的规律,排在氢前面的金属能与酸发生置换反应产生氢气,而金属之间的置换反应也遵循一定的顺序,这不仅有助于解释众多化学现象,还在实际应用中发挥着重要作用,如金属的冶炼、防锈处理等,深入理解金属活动性顺序表完整版,是开启化学知识宝库的一把关键钥匙。
在化学的广袤世界中,金属活动性顺序表完整版宛如一把神奇的钥匙,开启了理解金属化学性质的大门,它是化学学习中至关重要的工具,对于预测化学反应的方向、理解金属间的置换反应以及探索许多重要的化学现象都具有不可替代的作用。
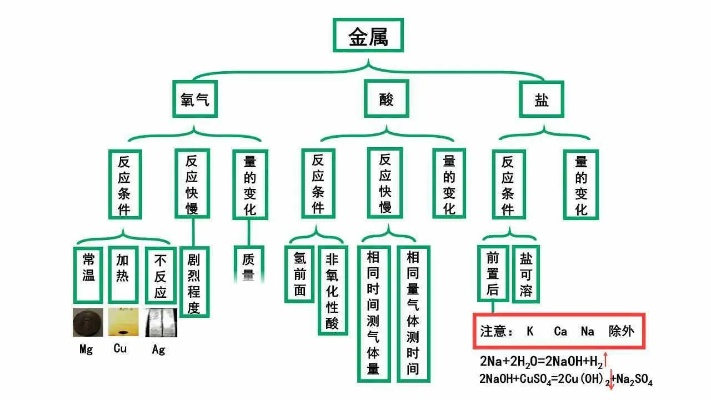
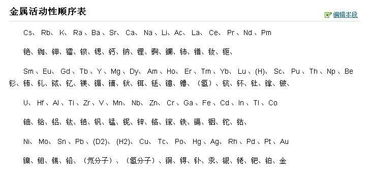
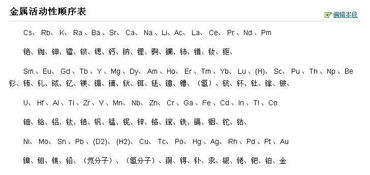
金属活动性顺序表完整版通常按照金属在水溶液中失去电子的难易程度进行排列,从左到右,金属的活动性逐渐减弱,排在前面的金属具有较强的还原性,能够从位于其后的金属盐溶液中置换出该金属,铁(Fe)可以与硫酸铜(CuSO₄)溶液发生反应,将铜(Cu)置换出来,化学方程式为:Fe + CuSO₄ = FeSO₄ + Cu,这一反应生动地体现了金属活动性顺序表的应用。
为什么会有这样的顺序呢?这与金属原子的结构密切相关,金属原子的最外层电子数较少,容易失去电子形成阳离子,金属的活动性越强,意味着它越容易失去电子,而电子的得失能力又与原子半径、核电荷数等因素有关,原子半径越大,核电荷数越小,金属原子越容易失去电子,其活动性就越强。
在金属活动性顺序表完整版中,钾(K)、钙(Ca)、钠(Na)等金属非常活泼,它们能够与水剧烈反应,产生氢气和相应的碱,钠投入水中会迅速游动,发出嘶嘶声,并生成氢氧化钠(NaOH)和氢气(H₂),而镁(Mg)、铝(Al)等金属则相对较活泼,它们可以与酸发生反应,但与水的反应相对较慢,锌(Zn)、铁(Fe)等金属的活动性较弱,只有在较强的酸存在下才会发生明显的反应,铜(Cu)、汞(Hg)、银(Ag)等金属则更加不活泼,一般情况下不与酸发生反应,但可以与某些氧化性较强的物质发生反应。
金属活动性顺序表完整版的应用非常广泛,在工业生产中,它可以帮助我们选择合适的金属材料来制造各种物品,对于需要耐腐蚀性的场合,我们可以选择活动性较弱的金属,如不锈钢(主要成分是铁、铬、镍等),在湿法冶金中,通过利用金属活动性的差异,可以从矿石中提取金属,用锌从含银的矿石中置换出银,金属活动性顺序表还可以帮助我们理解许多生活中的化学现象,如铁的生锈、铜器的表面变黑等。
金属活动性顺序表完整版并不是绝对的,在某些特殊情况下,金属的活动性可能会发生变化,在高温或有特殊催化剂存在的条件下,一些原本不活泼的金属可能会表现出较强的活性,金属的纯度、溶液的浓度、温度等因素也会对金属的活动性产生影响。
在学习金属活动性顺序表完整版时,我们需要通过实验来加深理解,通过观察金属与酸的反应现象、金属之间的置换反应等实验,可以直观地感受到金属活动性的差异,我们还需要结合理论知识,深入理解金属活动性的本质原因。
金属活动性顺序表完整版是化学学习中不可或缺的重要内容,它不仅是理解金属化学性质的基础,也是解决许多实际化学问题的有力工具,通过不断地学习和探索,我们可以更好地掌握这一知识体系,为今后的学习和研究打下坚实的基础,让我们一起走进金属活动性顺序表完整版的奇妙世界,去发现更多的奥秘吧!









 京公网安备11000000000001号
京公网安备11000000000001号 沪ICP备19017178号-1
沪ICP备19017178号-1
还没有评论,来说两句吧...